COVID-19藥增舒冠效 重度腎功能不全可用倍拉維
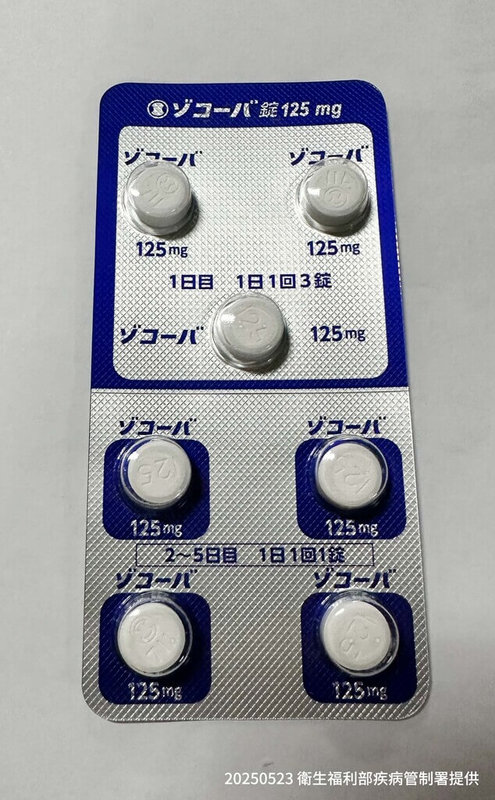
(中央社記者曾以寧台北23日電)此波COVID-19疫情急又猛,衛福部疾管署今天表示,日本新口服藥舒冠效(Xocova),已修訂用藥指引,作為口服替代藥使用;倍拉維亦已開放重度腎功能不全病人減量使用。
衛福部疾管署發言人羅一鈞今天接受媒體聯訪表示,此波COVID-19疫情又急又猛,有倍增趨勢,預計6月中下旬達疫情高峰時單週就診人次上看10萬。
對於藥物整備,羅一鈞今天說明,尚有瑞德西韋20.6萬劑、倍拉維46.9萬人份、莫納皮拉韋1萬人份。日本首款國產COVID-19口服藥、由藥廠塩野義製藥(Shionogi)研發的舒冠效(Xocova),亦已於15日修訂用藥指引、開放使用。
羅一鈞說明,適用對象為,無法使用倍拉維或瑞德西韋 (Remdesivir)的具任一重症風險因子(除懷孕外),未使用氧氣且於發病3天內大於等於12歲以上輕症病人。或機構群聚事件中,具任一重症風險因子(除懷孕外)的確診個案。
羅一鈞說明,目前舒冠效角色與莫納皮拉韋(Molnupiravir)一樣,為口服替代用藥,尤其針對莫納皮拉韋EUA期滿並將陸續屆效,若後續用罄,就會以舒冠效銜接使用;國內庫存有5000人份,並還有開口合約,屆時會視疫情需求適時叫貨。
羅一鈞解釋,過去倍拉維(Paxlovid)仿單並未註記洗腎病人、嚴重腎功能不全者使用劑量,因此不建議使用,多以莫納皮拉韋代替;不過近期藥廠基於後續實證資料,向食品藥物管理署提出倍拉維減量使用的方法,已經審查通過並加注於仿單,因此已發布通函通知醫界。
疾管署說明,食品藥物管理署已於114年2月25日核准倍拉維(Paxlovid)仿單變更,增列重度腎功能不全病人(eGFR<30mL/min,包含接受血液透析者)用法用量;未來遇重度腎功能不全(包含血液透析)病人經COVID-19檢驗陽性欲評估及開立口服抗病毒藥物時,可依最新核准用法開立倍拉維減量使用。
疾管署說明,基於倍拉維在預防高風險感染病人的效能優於莫納皮拉韋,且治療可能引發傷害的疑慮少於莫納皮拉韋,因此強烈建議針對非重症但有高住院風險之COVID-19感染病人,原則以倍拉維為治療首選藥物。1140523