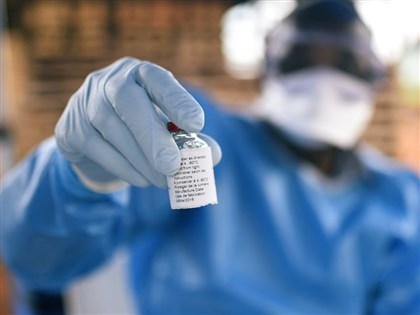
聯亞疫苗試驗主持人:擬台印雙邊進行3期試驗
(中央社記者江慧珺台北16日電)聯亞COVID-19疫苗未通過EUA審查,聯亞疫苗臨床試驗總主持人黃高彬今天透露,聯亞疫苗的中和抗體數據未與審查標準差太多,未來擬在台灣與印度雙邊進行第3期臨床試驗。
中央流行疫情指揮中心公布,聯亞COVID-19(2019 冠狀病毒疾病)疫苗與對照組阿斯特捷利康(AZ)疫苗的中和抗體數據相比,未能夠達到緊急使用授權(EUA)的療效評估基準,因此未能通過EUA。指揮官陳時中也坦言「很遺憾」。
中國醫藥大學附設醫院感染管制中心副院長、聯亞疫苗臨床試驗總主持人黃高彬接受媒體電話訪問表示,疫苗不只看中和抗體效價,還要考量T細胞反應,才是長期保護的重中之重。
黃高彬也透露,聯亞疫苗的中和抗體效價與血清反應比例數據,距離EUA的審查標準並沒有差太多,但也只能按照先前的規則。
至於聯亞COVID-19疫苗的下一步,黃高彬透露,因衛生福利部同意在台灣進行第3期臨床試驗,而印度也完成3期臨床試驗簽約,因此可能台灣與印度雙邊同時進行,若第3期臨床試驗結果出爐,可能直接申請正式藥證。
黃高彬表示,會進一步討論在台灣進行第3期臨床試驗的方式,可能也會採用免疫橋接的不劣性試驗,他表示,免疫橋接幾乎已是全世界同意的疫苗療效評估方法。(編輯:管中維)1100816
- 2025/10/08 10:15
- 2025/07/07 19:32
- 2024/08/12 17:30
- 2024/05/24 12:58
- 2024/02/02 13:19
- 2024/01/18 10:43
請繼續下滑閱讀